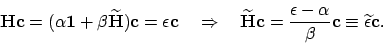Next: Symmetrie en groepentheorie
Up: Aantekeningen bij het college
Previous: Hybride orbitalen
Een eenvoudige MO beschrijving van geconjugeerde 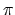 -systemen kunnen we verkrijgen met de zgn. Hückel-benadering. Deze benadering is erg grof, en levert dus ook niet echt kwantitatief goede resultaten, maar de symmetrie in het systeem komt er meestal goed uit. Stel, we bekijken een geconjugeerd
-systemen kunnen we verkrijgen met de zgn. Hückel-benadering. Deze benadering is erg grof, en levert dus ook niet echt kwantitatief goede resultaten, maar de symmetrie in het systeem komt er meestal goed uit. Stel, we bekijken een geconjugeerd 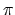 -systeem op atomen
-systeem op atomen
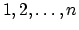 ,
met elektronen in de orbitalen
,
met elektronen in de orbitalen
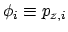 .
Aangezien we hier MO-theorie gaan doen zijn we geïnteresseerd in de matrix-elementen van de effectieve één-elektron Hamiltoniaan
.
Aangezien we hier MO-theorie gaan doen zijn we geïnteresseerd in de matrix-elementen van de effectieve één-elektron Hamiltoniaan
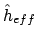 en de overlap. De Hückel-benadering houdt nu het volgende in:
en de overlap. De Hückel-benadering houdt nu het volgende in:
ofwel, alle overlap tussen de atomaire orbitalen 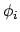 wordt verwaarloosd, en alle atomen worden als equivalent behandeld. Voor het simpelst denkbare
wordt verwaarloosd, en alle atomen worden als equivalent behandeld. Voor het simpelst denkbare 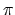 -systeem, etheen, krijgen we dan voor de matrix van
-systeem, etheen, krijgen we dan voor de matrix van
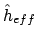
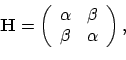 |
(74) |
en voor de overlap-matrix natuurlijk
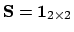 .
Oplossen van de seculiere vergelijkingen hiervoor is simpel:
.
Oplossen van de seculiere vergelijkingen hiervoor is simpel:
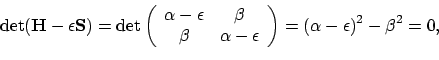 |
(75) |
ofwel
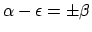 ,
zodat
,
zodat
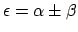 .
De bijbehorende MO's zijn dan ook snel genoeg gevonden door deze eigenwaarden in te vullen:
.
De bijbehorende MO's zijn dan ook snel genoeg gevonden door deze eigenwaarden in te vullen:
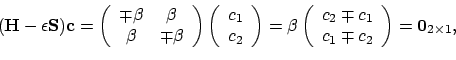 |
(76) |
zodat
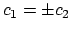 ,
en als we even aannemen dat
,
en als we even aannemen dat 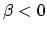 ,
dan hoort de symmetrische combinatie bij de bindende MO, en de antisymmetrische bij de anti-bindende, zodat we na normering krijgen:
,
dan hoort de symmetrische combinatie bij de bindende MO, en de antisymmetrische bij de anti-bindende, zodat we na normering krijgen:
Als we geheel volgens het Aufbau-principe denken, dan krijgen we de meest stabiele toestand als we beide 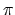 -elektronen in de bindende MO stoppen. Een schatting (en ook niet meer dan dat, zie ook hoofdstuk 5) voor de energie van die toestand kunnen we dan krijgen door de orbitaalenergieën van deze elektronen op te tellen, wat voor etheen resulteert in
-elektronen in de bindende MO stoppen. Een schatting (en ook niet meer dan dat, zie ook hoofdstuk 5) voor de energie van die toestand kunnen we dan krijgen door de orbitaalenergieën van deze elektronen op te tellen, wat voor etheen resulteert in
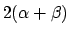 .
Stel dat we beide elektronen in hun atomaire orbitalen
.
Stel dat we beide elektronen in hun atomaire orbitalen 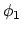 en
en 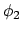 houden, dan geldt
houden, dan geldt 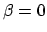 ,
zodat we dan voor de totale energie van het
,
zodat we dan voor de totale energie van het 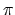 -systeem
-systeem 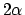 overhouden. Het verschil tussen deze twee energieën is de bindingsenergie van de
overhouden. Het verschil tussen deze twee energieën is de bindingsenergie van de 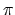 -binding. Definiëren we deze positief voor een bindende toestand, dan geldt dus voor de bindingsenergie van etheen
-binding. Definiëren we deze positief voor een bindende toestand, dan geldt dus voor de bindingsenergie van etheen
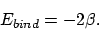 |
(79) |
Doen we hetzelfde voor butadieen, dan vinden we
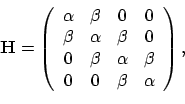 |
(80) |
met eigenwaarden
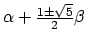 en
en
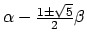 .
Definiëren we nu de bindingsenergie op dezelfde manier als bij etheen, dan vinden we
.
Definiëren we nu de bindingsenergie op dezelfde manier als bij etheen, dan vinden we
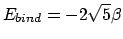 .
Stel nu dat we de
.
Stel nu dat we de 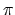 -bindingen op hun plaats hadden gehouden, ofwel de interactie tussen koolstofatomen 2 en 3 op nul haaden gezet. Dan had de Hamiltoniaan er uit gezien als 2 blokken
-bindingen op hun plaats hadden gehouden, ofwel de interactie tussen koolstofatomen 2 en 3 op nul haaden gezet. Dan had de Hamiltoniaan er uit gezien als 2 blokken
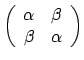 .
Maar daarvan kennen we de eigenwaarden, dit zijn namelijk de eigenwaarden van het losse etheenmolekuul. We hadden dan dus een bindingsenergie van
.
Maar daarvan kennen we de eigenwaarden, dit zijn namelijk de eigenwaarden van het losse etheenmolekuul. We hadden dan dus een bindingsenergie van 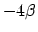 gevonden. Het verschil tussen de bindingsenergie van de totale, gedelocaliseerde beschrijving, en de bindingsenergie van de gelocaliseerde beschrijving kunnen we beschouwen als een maat voor de delocalisatie-energie van de
gevonden. Het verschil tussen de bindingsenergie van de totale, gedelocaliseerde beschrijving, en de bindingsenergie van de gelocaliseerde beschrijving kunnen we beschouwen als een maat voor de delocalisatie-energie van de 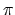 -binding, in het geval van butadieen dus
-binding, in het geval van butadieen dus
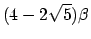 .
Meer algemeen kunnen we schrijven
.
Meer algemeen kunnen we schrijven
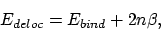 |
(81) |
waar n het aantal 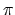 -bindingen is.
-bindingen is.
Op precies dezelfde manier kunnen we ook grotere 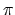 -systemen beschrijven. Hoewel de Hückel methode simpel genoeg is om met de hand te diagonaliseren, kan dit voor grotere systemen toch een tamelijk tijdrovend proces worden. Maar aangezien we meestal geen getallen voor
-systemen beschrijven. Hoewel de Hückel methode simpel genoeg is om met de hand te diagonaliseren, kan dit voor grotere systemen toch een tamelijk tijdrovend proces worden. Maar aangezien we meestal geen getallen voor 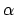 en
en 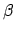 invullen, kunnen we de diagonalistie dus niet direct met een numeriek pakket (zoals bv. Matlab) uitvoeren. Willen we dit toch doen, dan moeten we het probleem eerst even herschrijven, door de
H-matrix te schrijven als
invullen, kunnen we de diagonalistie dus niet direct met een numeriek pakket (zoals bv. Matlab) uitvoeren. Willen we dit toch doen, dan moeten we het probleem eerst even herschrijven, door de
H-matrix te schrijven als
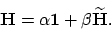 |
(82) |
Merk op dat
 alleen nog maar nullen en enen bevat. Omschrijven van het eigenwaarde-probleem levert ons
alleen nog maar nullen en enen bevat. Omschrijven van het eigenwaarde-probleem levert ons
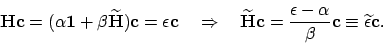 |
(83) |
Dus, door het eigenwaarde-probleem
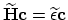 op te lossen (wat we gewoon met Matlab kunnen doen), krijgen we de eigenvectoren van
H, en de geschaalde eigenwaarden
op te lossen (wat we gewoon met Matlab kunnen doen), krijgen we de eigenvectoren van
H, en de geschaalde eigenwaarden
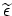 ,
waaruit we de eigenwaarden van
H kunnen reconstrueren door
,
waaruit we de eigenwaarden van
H kunnen reconstrueren door
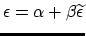 uit te rekenen.
uit te rekenen.



Next: Symmetrie en groepentheorie
Up: Aantekeningen bij het college
Previous: Hybride orbitalen
Gerrit Groenenboom
2005-06-01
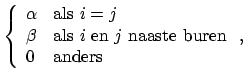
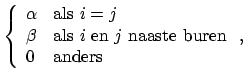
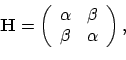
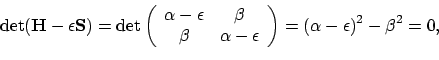
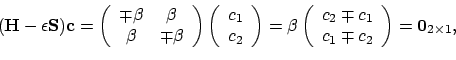
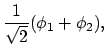
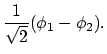
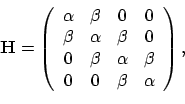
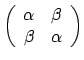 .
Maar daarvan kennen we de eigenwaarden, dit zijn namelijk de eigenwaarden van het losse etheenmolekuul. We hadden dan dus een bindingsenergie van
.
Maar daarvan kennen we de eigenwaarden, dit zijn namelijk de eigenwaarden van het losse etheenmolekuul. We hadden dan dus een bindingsenergie van ![]() -systemen beschrijven. Hoewel de Hückel methode simpel genoeg is om met de hand te diagonaliseren, kan dit voor grotere systemen toch een tamelijk tijdrovend proces worden. Maar aangezien we meestal geen getallen voor
-systemen beschrijven. Hoewel de Hückel methode simpel genoeg is om met de hand te diagonaliseren, kan dit voor grotere systemen toch een tamelijk tijdrovend proces worden. Maar aangezien we meestal geen getallen voor ![]() en
en ![]() invullen, kunnen we de diagonalistie dus niet direct met een numeriek pakket (zoals bv. Matlab) uitvoeren. Willen we dit toch doen, dan moeten we het probleem eerst even herschrijven, door de
H-matrix te schrijven als
invullen, kunnen we de diagonalistie dus niet direct met een numeriek pakket (zoals bv. Matlab) uitvoeren. Willen we dit toch doen, dan moeten we het probleem eerst even herschrijven, door de
H-matrix te schrijven als